化学方程式书写与应用(第3课时)(课件)-2022-2023学年九年级化学上册同步精品课堂(沪教版)


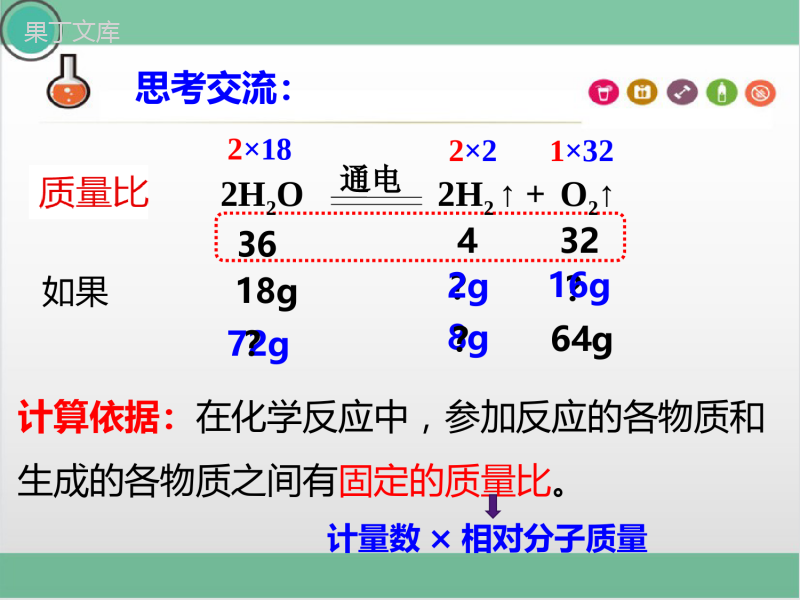

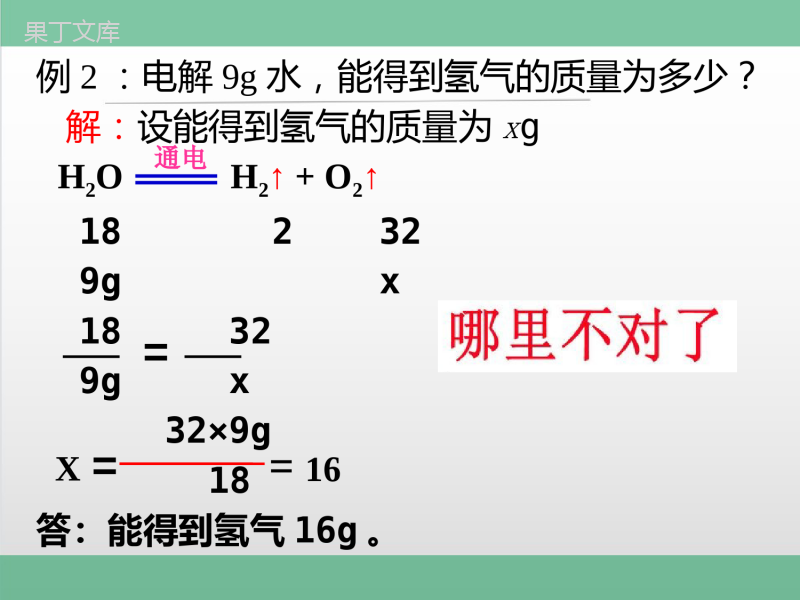
第4章认识化学变化第3节化学方程式的书写与应用(第3课时)【学习目标】2.认识定量研究对化学科学发展的意义。1.能利用化学方程式进行简单的计算。。36432计算依据:在化学反应中,参加反应的各物质和生成的各物质之间有固定的质量比。如果18g?8g?16g64g?72g?2g计量数×相对分子质量2×182×21×322H2O2H2↑+O2↑通电思考交流:g1836x4例1:18g水完全电解可产生多少克氢气?=(5)作答:(1)设未知量:①解:设产生氢气质量为x②2H2O2H2↑+O2↑通电(2)写化学方程式:(3)标出有关物质相对分子质量(不要忘乘化学计量数)及实际质量:③36418gX(4)列比例式,求解:X=2g④⑤答:产生氢气质量为2g。g1836x4例2:电解9g水,能得到氢气的质量为多少?解:设能得到氢气的质量为xgH2OH2↑+O2↑182329gx18329gx32×9g18答:能得到氢气16g。X==16通电=根据化学方程式计算步骤及格式:1.按题意设未知数2.写出题中反应的化学方程式3.找出反应物和生成物的质量关系4.建立已知量和未知量的比例关系5.计算x,并作答反应物和生成物的质量关系相对质量=分子个数×相对分子质量实际质量:数据要带单位已知量和未知量的比例关系相对质量实际质量上下相比比值相等1.两要领:(1)步骤要完整;(2)格式要规范。2.两关键:(1)书写化学方程式要准确;(2)相对分子质量计算要准确。化学方程式计算的要领和关键:解:设能得到氢气的质量为x2H2O2H2↑+O2↑通电3649gx369g4x=x=1g答:电解9g水,能得到氢气的质量为1g。思路1:利用化学方程式来计算例2:电解9g水,能得到氢气的质量为多少?理由:水中的氢元素全部转化为氢气解:9g水中所含氢元素的质量1×21×2+16×100%==1g思路2:根据化学式的计算9g×答:电解9g水,能得到氢气的质量为1g。例2:电解9g水,能得到氢气的质量为多少?例3:加热完全分解31.6g高锰酸钾,得到氧气质量多少克?2KMnO4K2MnO4+MnO2+O2↑△3163231.6gx3163231.6gx=x=3.2g解:设得到氧气质量为x答:得到氧气质量为3.2g。例4:加热31.6g高锰酸钾,当产生3.2g氧气时,固体剩余物的成分是()A.K2MnO4和MnO2B.KMnO4、K2MnO4和MnO2C.KMnO4和MnO2D.KMnO4和K2MnO432例5:足量的镁带在标准状况下与11.2L的氧气(密度为1.43g/L)充分燃烧,可以生成多少克氧化镁?体积不能直接代入方程式计算,代入量必须是质量2Mg+O22MgO点燃328011.6Lx例5:足量的镁带在标准状况下与11.2L的氧气(密度为1.43g/L)充分燃烧,可以生成多少克氧化镁?328011.2L×1.43g/Lx解:设可以生成多少克氧化镁的质量为x2Mg+O22MgO点燃328011.2L×1.43g/Lx=x=40g答:可以生成氧化镁的质量为40g。例6:将氯酸钾、二氧化锰的混合物26g,加热至完全反应,得剩余固体的质量为16.4g。求:(1)则生成的氧气质量为多少g?(2)原混合物中有多少g氯酸钾?26gKClO2MnO2KClO3MnO2剩余固体16.4g26g-16.4g=9.6g反应前反应后=26g16.4g26g26g代入方程式的量是纯物质质量,不能是混合物质量2KClO32KCl+3O2↑MnO2解:26g-16.4g=9.6gO2m=(1)(2)设原混合物中氯酸钾质量为x二氧化锰质量?26g-24.5g=1.5g例6:将氯酸钾、二氧化锰的混合物26g,加热至完全反应,得剩余固体的质量为16.4g。求:(1)则生成的氧气质量为多少g?(2)原混合物中有多少g氯酸钾?2KClO32KCl+3O2↑MnO224596x9.6g24596x9.6g=x=24.5g答:原混合物中氯酸钾的质量为24.5g。(1)各代入量均是纯净物的质量;(2)计算过程中单位要统一;(3)注意“充分反应”“恰好完全反应”“适量”等词。化学方程式计算的要领和关键:【中考链接】1.(2022·山东菏泽)我国古代将炉甘石(主要成分ZnCO3)和木炭粉混合后加热到约800℃,可得到锌。主要发生的化学反应:某同学用100t含ZnCO398%的炉甘石,计算生成ZnO质量的过程如下,请判断该计算过程是否正确?3ZnCOZnO+CO12581100tx高温125100t81x=64.8tx答:可得到氧化锌的质量是64.8t。②C+ZnO2ZnO+CO2↑高温①ZnCO3ZnO+CO2↑高温解:设可得到氧化锌的质量为x3ZnCOZnO+CO12581100tx高温125100t81x=64.8tx【中考链接】2.(2022·湖南衡阳)以下是某同学解答一道计算题的过程:题目:将氯酸钾和二氧化锰的混合物共27.5g放入试管中加热,反应中剩余固体质量与反应时间的关系如图所示。完全反应后,生成氯化钾的质量是多少?该同学很快列出计算过程,求出了氯化钾的质量。请你帮该同学检查是否正确。解:设生成KCl的质量为x232MnO2KClO2KCl+3OΔ122.574.527.5gx122.574.5=27.5gxx=16.7g答:生成KC1的质量为16.7g。232MnO2KClO2KCl+3OΔ122.574.527.5gx122.574.5=27.5gx
提供化学方程式书写与应用(第3课时)(课件)-2022-2023学年九年级化学上册同步精品课堂(沪教版)会员下载,编号:1701028513,格式为 xlsx,文件大小为18页,请使用软件:wps,office Excel 进行编辑,PPT模板中文字,图片,动画效果均可修改,PPT模板下载后图片无水印,更多精品PPT素材下载尽在某某PPT网。所有作品均是用户自行上传分享并拥有版权或使用权,仅供网友学习交流,未经上传用户书面授权,请勿作他用。若您的权利被侵害,请联系963098962@qq.com进行删除处理。

 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载