《影响化学反应速率的因素》人教版高二化学选修4PPT课件.pptx



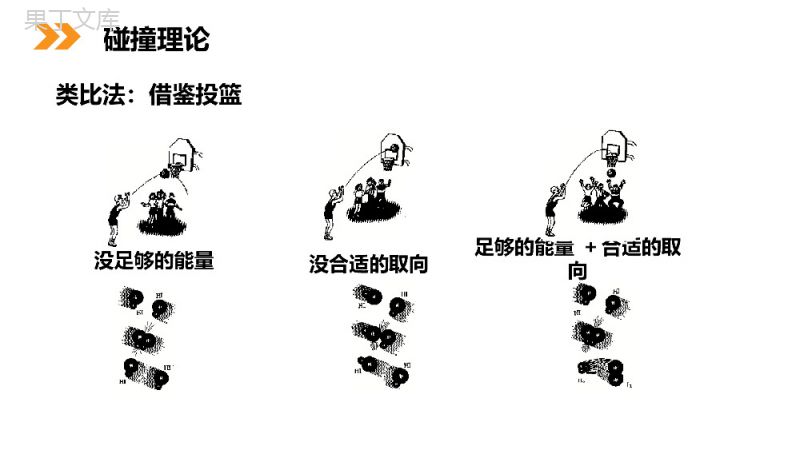
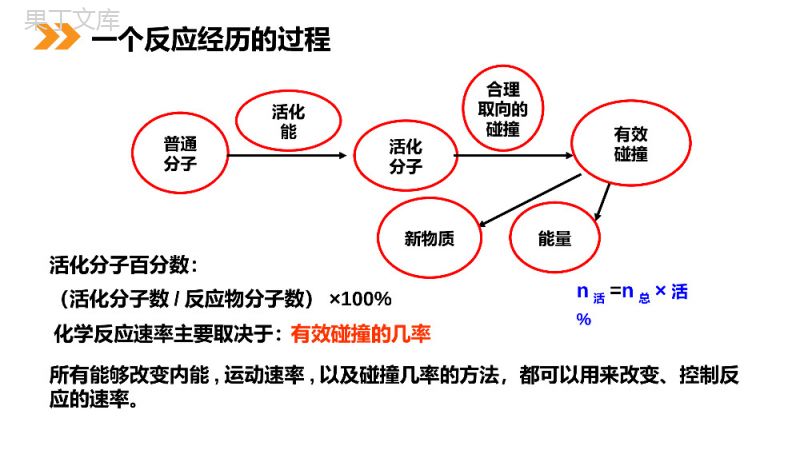
教师:68素材MENTALHEALTHCOUNSELINGPPT第2节影响化学反应速率的因素第二章化学反应速率和化学平衡人教版高中化学选修4(高二)课前引入在通常情况下,Na与水的反应和Mg与水的反应哪个剧烈(反应速率快)?为什么?这说明化学反应速率的决定因素是什么?内因:物质本身的结构和性质是化学反应速率大小的决定因素,反应类型不同有不同的化学反应速率,反应类型相同但反应物不同,化学反应速率也不同。影响反应速率的因素(1)内部因素(主要因素):参加反应物质的性质(2)外部因素:①浓度:②压强:③温度:④催化剂:⑤其他因素:光、颗粒大小、溶剂等。课前引入没合适的取向没足够的能量足够的能量+合适的取向类比法:借鉴投篮碰撞理论n活=n总×活%活化分子百分数:(活化分子数/反应物分子数)×100%化学反应速率主要取决于:所有能够改变内能,运动速率,以及碰撞几率的方法,都可以用来改变、控制反应的速率。普通分子活化能活化分子合理取向的碰撞有效碰撞新物质能量有效碰撞的几率一个反应经历的过程浓度增大→单位体积内n总↑T不变,活%不变n活增大→有效碰撞↑→V↑1、在其他条件不变时,增大反应物浓度,可以增大反应速率实验2-2结论:浓度大的H2C2O4(aq)先褪色2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O规律:其他条件不变时,增大反应物的浓度,可以增大反应速率;减小反应物的浓度,可以减小化学反应的速率。一、浓度对反应速率的影响本质原因反应物浓度增大,单位体积内活化分子数增多,有效碰撞的频率增加,反应速率增大。浓度对反应速率的影响a、此规律只适用于气体或溶液的反应,对于纯固体或液体的反应物,一般情况下其浓度是常数,因此改变它们的量一般不会改变化学反应速率。c、随着化学反应的进行,反应物的浓度会逐渐减小,因此一般反应速率也会逐渐减小。典例1:一定条件下,在CaCO3(块状)+2HCl=CaCl2+H2O+CO2反应中,为了加快反应的速率,下列那些方法可行()A、增加HCl的浓度B、加水C、增加同浓度盐酸的量D、改加CaCO3粉末b、一般来说,固体反应物表面积越大,反应速率越大,固体反应物表面积越小,反应速率越小。AC注意:原因:对气体来说,若其他条件不变,增大压强,就是增加单位体积的反应物的物质的量,即增加反应物的浓度,因而可以增大化学反应的速率。请试根据浓度对化学反应速率的影响推出压强对化学反应速率的影响情况二、压强对反应速率的影响规律:对于有气体参加的反应,若其他条件不变,增大压强,气体体积缩小,浓度增大,反应速率加快;减小压强,反应速率减慢。压强增大→体积减小其他条件不变→V↑→C增大压强对于反应速率的影响是通过对浓度的影响实现的P增大→C成比例增大,P减小→C成比例减小压强只对于有气体参加的反应的速率有影响发散思考:压强对于任意化学反应的速率都有影响吗?二、压强对反应速率的影响思考:在N2+3H22NH3中,当其他外界条件不变时:Ⅰ减小体系压强,该反应的速率怎么变?Ⅱ在反应中保持体系容积不变,充入N2,反应的速率怎么变?Ⅲ在反应中保持体系容积不变,充入He,反应的速率怎么变?Ⅳ在反应中保持体系压强不变,充入He,反应的速率怎么变?压强影响反应速率,必须伴随有压强改变时体积的改变现象。否则,压强的变化并没有作用到反应的体系上。即压强变则体积变,实际是浓度的变化。若容器的体积不变,因为各气体的浓度没有变,则速率不变。如在密闭容器中通入惰性气体。注意:二、压强对反应速率的影响1、恒温时:增大压强→体积减少→C增大→反应速率增大2、恒容时:A、充入气体反应物→反应物浓度增大→总压增大→反应速率增大;B、冲入“无关气体”(如He、N2等)→引起总压增大,但各反应物的分压不变,各物质的浓度不变→反应速率不变3、恒压时:冲入“无关气体”(如He等)→引起体积增大,→各反应物浓度减少→反应速率减慢。对于气体有下列几种情况:典例2对于反应N2+O2=2NO在密闭容器中进行,下列条件哪些不能加快该反应的化学反应速率()A、缩小体积使压强增大B、体积不变充入N2使压强增大C、体积不变充入O2使压强增大D、使体积增大到原来的2倍E、体积不变充入氦气使压强增大DE典型例题实验2-3结论:温度高的溶液先出现浑浊Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O1、其他条件不变,温度升高,反应速率加快T↑→普通分子变为活化分子→活%↑→n活↑→V↑2、一般说来,温度每升高10℃,速率增加2-4倍。V×倍数值(t2-t1)/10=变化后的反应速率3、温度对反应速率影响的规律,对吸热反应,放热反应都适用。4、反应若是可逆反应,升高温度,正、逆反应速率都加快,降低温度,正、逆反应速率都减小。三、温度对反应速率的影响冰箱延长食物保鲜期你能举出生活中利用改变温度改变反应速率的例子吗实验2-4结论:加入催化剂可以加快反应的速率四、催化剂对反应速率的影响使用催化剂,能够降低反应所需的能量,这样会使更多的反应物的分子成为活化分子,大大增加单位体积内反应物分子中活化分子所占的百分数。因而使反应速率加快。催化剂:能改变化学反应速率而自身的化学组成和质量在反应前后保持不变催化剂正催化剂负催化剂加快化学反应速率减慢化学反应速率注:不说明指正催化剂四、催化剂对反应速率的影响能量反应过程E1E2反应物生成物活化分子活化能活化分子变成生成物分子放出的能量反应热没加催化剂加了催化剂四、催化剂对反应速率的影响(1)凡是能改变反应速率而自身在化学变化前后化学性质和质量没有发生变化的物质叫催化剂。(2)使用催化剂同等程度的增大(减慢)正逆反应速率,从而改变反应到达平衡所需时间。(3)没特别指明一般指正催化剂(4)催化剂只能催化可能发生的反应,对不发生的反应无作用(4)催化剂一定的具有选择性(5)催化剂中毒:催化剂的活性因接触少量的杂质而明显下降甚至遭到破坏,这种现象叫催化剂中毒。(6)生物催化剂酶是蛋白质,温度过高会发生变性。注意:各条件对速率的影响大小是:催化剂>>温度>浓度=压强(体积变化引起的)。各种影响都有其局限性,要针对具体反应具体分析。总结:五、其他如光照、反应物固体的颗粒大小、电磁波、超声波、溶剂的性质等,也会对化学反应的速率产生影响。影响因素分子总数活化分子百分数活化分子总数活化分子浓度(单位体积活化分子数)增大浓度增大压强升高温度正催化剂增加不变不变不变不变不变增加增加增加增加增加增加增加增加增加不变外界条件对化学反应速率的影响(总结)练习1:对于在溶液间进行的反应,对反应速率影响最小的因素是()A、温度B、浓度C、压强D、催化剂练习2:下列条件的变化,是因为降低反应所需的能量而增加单位体积内的反应物活化分子百分数致使反应速率加快的是()A、增大浓度B、增大压强C、升高温度D、使用催化剂CD典型例题感谢您下载68素材平台上提供的PPT作品,为了您和68素材以及原创作者的利益,请勿复制、传播、销售;素材均来源于网络用户分享,故68素材不具备充分的监控能力来审查图片是否存在侵权等情节。68素材不拥有此类图片的版权,本站所有资源仅供学习与交流,不得用于任何商业用途的范围,用户应自觉遵守著作权法及其他相关法律的规定,不得侵犯本网站及权利人的合法权利,给68素材和任何第三方造成损失的,侵权用户应负全部责任。版权声明练习3:设NO+CO22CO(正反应吸热)反应速率为v1;N2+3H22NH3(正反应放热)反应速率为v2。对于前述反应,当温度升高时,v1和v2变化情况为()A、同时增大B、同时减小C、v1减少,v2增大D、v1增大,v2减小A典型例题教师:68素材MENTALHEALTHCOUNSELINGPPT感谢各位的仔细聆听第二章化学反应速率和化学平衡人教版高中化学选修4(高二)
提供《影响化学反应速率的因素》人教版高二化学选修4PPT课件.pptx会员下载,编号:1701021387,格式为 xlsx,文件大小为25页,请使用软件:wps,office Excel 进行编辑,PPT模板中文字,图片,动画效果均可修改,PPT模板下载后图片无水印,更多精品PPT素材下载尽在某某PPT网。所有作品均是用户自行上传分享并拥有版权或使用权,仅供网友学习交流,未经上传用户书面授权,请勿作他用。若您的权利被侵害,请联系963098962@qq.com进行删除处理。

 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载