人教版九年级化学(第三单元物质构成的奥秘)复习课件(PPT共40张)


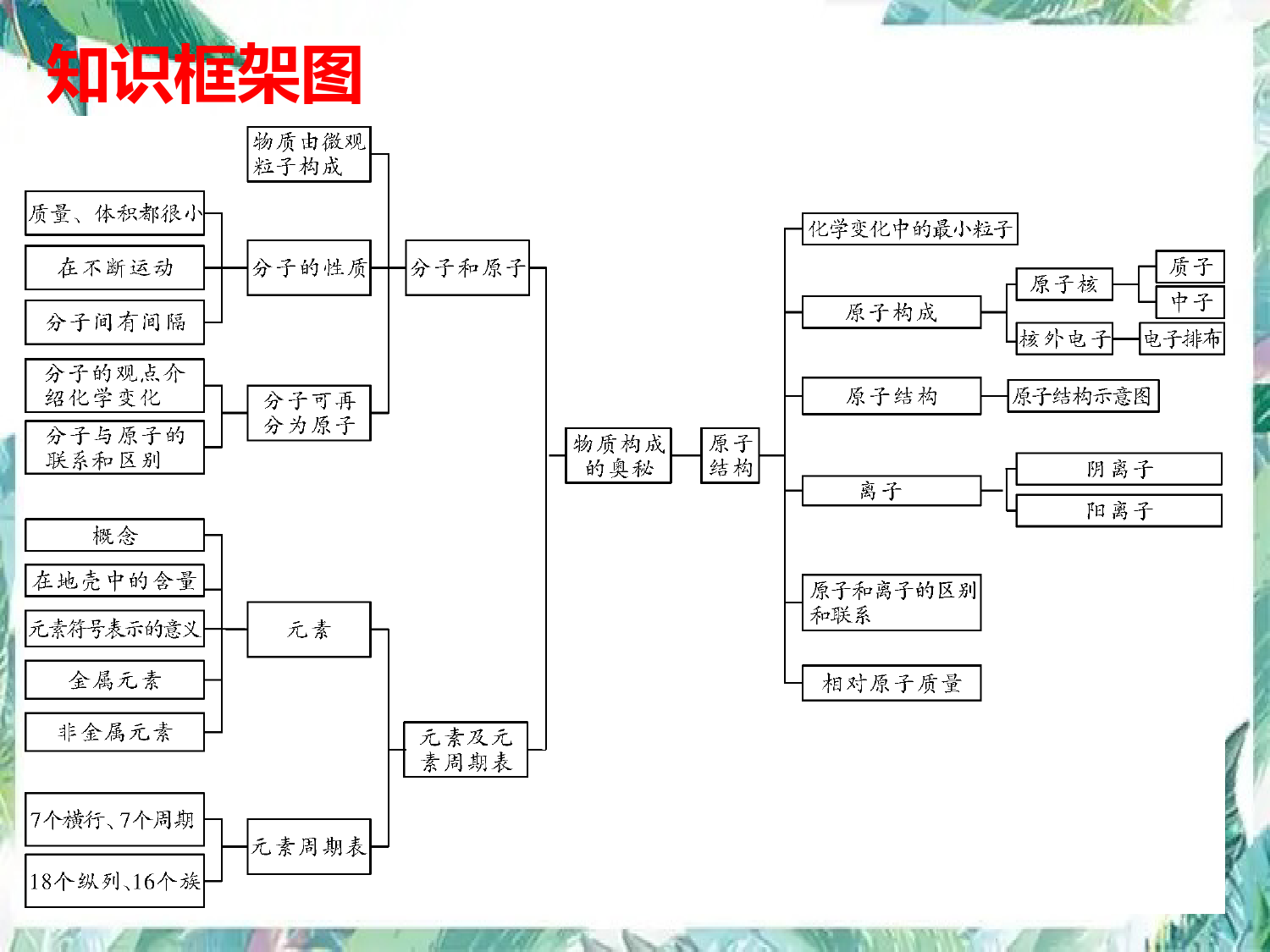
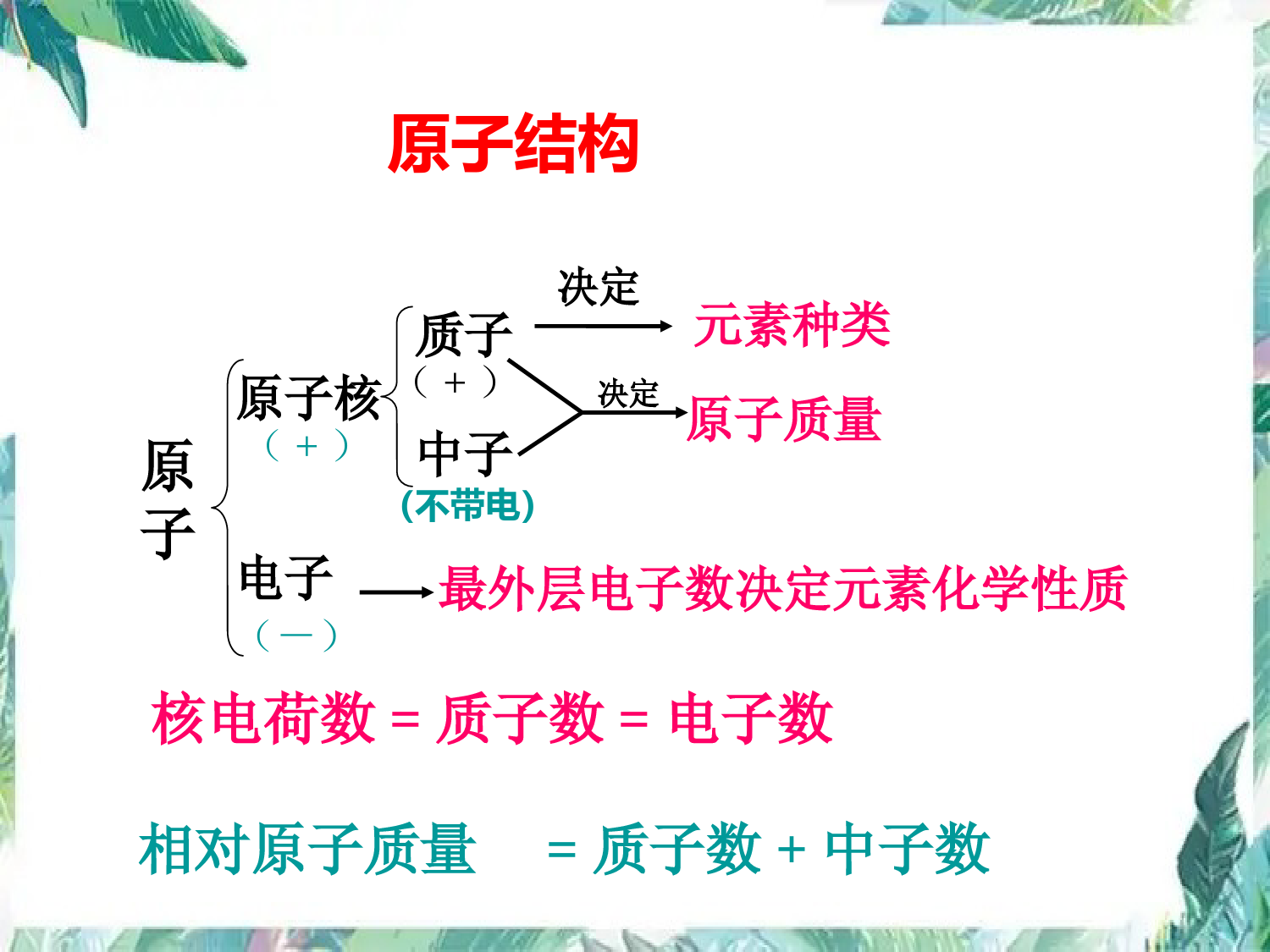

第3单元《物质构成的奥秘》期末总复习复习目标1、知道原子是由原子核和核外电子构成的。2、知道分子、原子、离子的区别。3、知道原子可以结合成分子、同一元素的原子、离子可以相互转化。4、会用微粒的观点解释生活中的现象。知识框架图原子核电子质子中子决定元素种类最外层电子数决定元素化学性质决定原子质量(+)(-)(+)(不带电)核电荷数=质子数=电子数相对原子质量=质子数+中子数原子原子结构原子结构原子构成的规律:⑴、原子核所带的电荷数简称为核电荷数⑵、核电荷数=质子数=核外电子数⑶、质子数不一定等于中子数⑷、原子中不一定含有中子⑸、不同种类的原子,其核内质子数和核外电子数都不相同(6)原子的质量主要集中在原子核上据中央电视台6月3日对云南抚仙湖湖底古城考古的现场报道,科学家曾通过测定古生物遗骸的碳14含量来推断古城年代。碳14原子的核电荷数为6,相对原子质量为14。下列关于碳14原子的说法中,错误的是()A、中子数为6B、质子数为6C、电子数为6D、质子数与中子数的和为14练一练A我国”嫦娥工程”探月计划的一个重要目标是开发月球新能源氦—3。10吨氦—3就能满足我国一年的所有的能源需求。关于氦—3的说法正确的是()A质子数为3电子数为3B质子数为2,电子数为2C质子数为2电子数为3D质子数为3,电子数为2B练习(1)原子核()。A.由电子和质子构成B.由质子和中子构成C.由电子和中子构成D.由质子、中子和电子构成(2)在原子里质子数等于()。A.中子数B.电子数C.中子数与电子数之和D.中子数与电子数之差(3)碳的相对原子质量是()。A.12gB.12C.1.6610-27kgD.1/12g(4)现有质量相同的钠、镁、铝三块金属,哪一种金属含的原子最多?哪一种金属含的原子最少?为什么?解:已知Na,Mg,Al的相对原子质量分别是23、24、27。又因为相对原子质量越大,则该原子实际质量越大,故得一个钠原子的质量最小,一个铝原子的质量最大。现Na,Mg,Al的质量相等,故含有的钠原子的个数最多。含铝原子数最少。(即用质量除以每一个原子质量得原子数)。BBB离子就是带电的原子或原子团。是原子得失电子而形成一种的粒子。跟原子、分子一样,离子也是构成物质的一种粒子。离子稀有气体元素,如氖(Ne)、氩(Ar)等,它们最外层电子都是8个(氦(He)为2个)。由于它们均不易与其他物质发生化学反应,呈现“化学惰性”,所以认为最外层具有8电子(只有一个电子层的具有2个电子)的结构,属于相对稳定结构。金属元素,如钠、镁、铝等,最外层电子一般4个,在化学反应中易电子,趋向达到相对稳定结构。非金属元素,如氧、氯、硫等,最外层电子一般4个,在化学反应中易电子,趋向达到相对稳定结构。小于失去大于得到在化学反应中,失去最外层电子,带正电荷的原子叫做;得到电子,带负电荷的原子叫做。阳离子阴离子例如:H+、Na+、Mg2+、Al3+、Cl-、O2-、S2-1、下列微粒是阳离子的有();是阴离子的有()是原子的有();为稳定结构的有()ABCDABCDBCD2、下列原子的电子层排布相同的是()2.3.63、元素X核电荷数为a,它的阳离子Xm+与Y的阴离子Yn-的电子层结构相同,则元素Y的核电荷数()A.m+n+aB.m-n-aC.m+n-aD.a-m-nDOH-NO3-SO42-CO32-NH4+常见的原子团离子4、在Na+.、F-、O2,-、H2O、NH4+、Mg2+、OH-七种粒子中,相同的是()A质子数B电子数C中子数D原子数B讨论?在化学变化中分子发生了变化,那么构成分子的原子是否也发生变化?在化学变化中,发生变化的是分子,原子没有发生变化。原子是化学变化中的最小粒子分子是一种保特物质化学性质的最小粒子。分子有哪些基本性质呢?1、同种分子化学性质相同;2、分子体积小,质量小;4、分子间存在相互作用,在不停地运动;3、分子之间有间隙;什么是分子?学习了微粒的性质,明明在家做了个实验,验证微粒的性质。将一个透明玻璃杯装上水,放入一大块冰糖,用细线记录下水位(如图所示)。过一段时间观察到的现象:(1),说明;(2),说明。冰糖消失微粒不断运动液面下降微粒间有空隙练一练2、从分子的角度分析水的蒸发与水的分解两种变化的不同之处。物质的构成物质分子构成离子构成原子构成构成组成元素总称宏观概念微观概念(只讲种类不讲个数)(既讲种类又讲个数)分裂得失电子失得电子分子原子离子H2、O2、N2H2O、CO2等金属:如Fe稀有气体:如He金刚石(C)等NaCl、KCl等我能构成哪些物质?表示方法:化学式表示方法:元素符号表示方法:离子符号元素就是具有相同核电荷数(即核内质子数)的一类原子的总称。什么是元素?元素与原子的比较练习(1)不同种元素最本质的区别是()。A.质子数不同B.中子数不同C.相对原子质量不同D.中子数与核外电子数之和不同(2)地壳中含量最多的元素是()。A.氧B.铁C.铝D.钙(3)地壳中含量最多的金属元素是()。A.硅B.铁C.铝D.钙(4)写出氮、氯、硫、磷、锰、铜、金的元素符号。(5)写出He、F、Si、K、Ag、Hg的元素名称。(6)将下列写错的元素符号加以改正:铜CU,锌ZN,银AG,氯cl,钙cAAAC1.将零散的化学知识整理归纳,得出一般的规律,是学好化学的可取方法之一。物质的组成、结构和性质关系归纳错误的是()A.核内质子数决定了元素的种类B.元素的化学性质与原子最外层电子数目关系密切C.原子是化学反应中最小的粒子,因此原子不可再分D.物质是由分子、原子、离子等粒子构成练习C1、下列微粒的性质与质子数、电子数、中子数、电子层数、最外层电子数等有关,请你用它们填空元素种类_____________;相对原子质量_____________;元素的化学性质___________;离子所带电荷数___________;质子数质子数、中子数最外层电子数最外层电子数2、物质的组成、结构和性质的关系中,不正确的是()A、核内质子数决定元素的种类B、元素的化学性质与原子的最外层电子数关系密切C、具有相对稳定结构的粒子一定是稀有气体元素的原子D、镁离子和氧离子的核外电子数相同C3、保持氧气化学性质最小的微粒是()A.O2B.OC.O2-D.H2OA4.1999年度诺贝尔化学奖获得者艾哈迈德·泽维尔,开创了“飞秒(10-15)化学”的新领域,使运用激光光谱技术观测化学反应时分子中原子的运动成为可能,你认为该技术不能观察到的是()A.化学变化中反应物分子的分解B.反应中原子的运动C.化学变化中生成物分子的形成D.原子核的内部结构D物质构成练习汞原子二氧化碳分子钠离子、氯离子6、用化学符号表示:2个氮原子2个氮分子2个铁离子2个亚铁离子2个铁原子n个水分子2N2N22Fe3+2Fe2+2FenH2ONH4+2OH-5、科学研究证实,物质是由微粒构成的,例如铁是由铁原子构成的。请你填写构成下列物质的具体微粒的名称。⑴体温计中的汞是由构成的;⑵人工降雨用的干冰是由构成的;⑶食盐中的氯化钠是由构成的。最外层电子7.对于Fe、Fe2+、Fe3+三种微粒的判断,正确的是()①核电荷数相同②核外电子数相等③电子层结构完全相同④质量几乎相等⑤等质量的三种微粒所含的质子数相等⑥三种粒子的化学性质相似A.①④⑤B.①③⑤C.②③④D.①②③④⑤⑥A电子层该电子层上的电子数原子核核内质子数(核电荷数)Na原子结构示意图本单元考点分析:考点一:结构示意图核电荷数=质子数=电子数(分子、原子)核电荷数=质子数≠电子数(离子)相对原子质量≈质子数+中子数元素种类由_________决定,元素化学性质主要由_____________决定,元素的相对原子质量由_____________决定。原子的质子数原子的最外层电子数质子数和中子数的和1.(2019河北)压缩气体可使气体液化,气体液化后()A.分子的质量变大B.分子的体积变小C.分子的数目减少D.分子的间隙变小D•⒈物质由元素组成。•⒉物质由粒子(分子、原子、离子)构成。例如:⑴水是由水分子构成的。⑵金是由金原子构成的。⑶氯化钠是由钠离子和氯离子构成的。•⒊分子是由原子构成的。物质组成、构成的描述考点二2.(2019山西)我国“高分5号”卫星天线是用钛镍形状记忆合金制成的。如图为镍的原子结构示意图,关于该原子的叙述错误的一项是()A.它的核电荷数为28B.它有4个电子层C.它的质子数大于核外电子数D.它易失电子D3.(2019深圳)钪(Sc)是一种“工业的维生素”。图为钪在元素周期表中的相关信息及其原子的结构示意图。下列说法正确的是()A.钪属于非金属元素B.钪的相对原子质量是21C.原子结构示意图中x=10D.钪原子核外有四个电子层D4.(2019郴州)下列说法正确的是()A.分子是化学变化中的最小粒子B.原子核是由质子和电子构成C.NaCl由NaCl分子构成D.水蒸发过程中,水分子间隔变大D5.(2019铁岭)下图中A是锡元素在元素周期表中的信息,B~E是四种粒子的结构示意图。请回答:(1)锡元素属于____(填“金属”或“非金属”)元素。(2)锡元素的相对原子质量是。(3)D粒子在化学反应中容易____(填“得到”或“失去”)电子。(4)B、C、D、E四种粒子中属于同种元素的是(填字母,下同),具有相对稳定结构的是____。金属118.7失去CDBCE6.(2019福建)2019年是“国际化学元素周期表年”(1)中国科学院院士张青莲对铟、铱、锗等的相对原子质量的测定做出了杰出贡献。锗元素在元素周期表中的部分信息如图所示,锗的相对原子质量为____,该元素属于____(填“金属元素”或“非金属元素”)。(2)中国科学家姜雪峰当选为“全球青年化学家元素周期表硫元素大使”。72.63金属元素K2S①如图是硫原子结构示意图,硫原子的最外层电子数是;硫离子的符号为____;硫离子与硫原子的化学性质____(填“相同”或“不同”)。②火药是中国古代四大发明之一。黑火药爆炸的反应为,X的化学式是____。6S2-不同
提供人教版九年级化学(第三单元物质构成的奥秘)复习课件(PPT共40张)会员下载,编号:1701028430,格式为 xlsx,文件大小为40页,请使用软件:wps,office Excel 进行编辑,PPT模板中文字,图片,动画效果均可修改,PPT模板下载后图片无水印,更多精品PPT素材下载尽在某某PPT网。所有作品均是用户自行上传分享并拥有版权或使用权,仅供网友学习交流,未经上传用户书面授权,请勿作他用。若您的权利被侵害,请联系963098962@qq.com进行删除处理。

 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载