《醇》人教版高二化学选修五PPT课件(第3.1.1课时).pptx


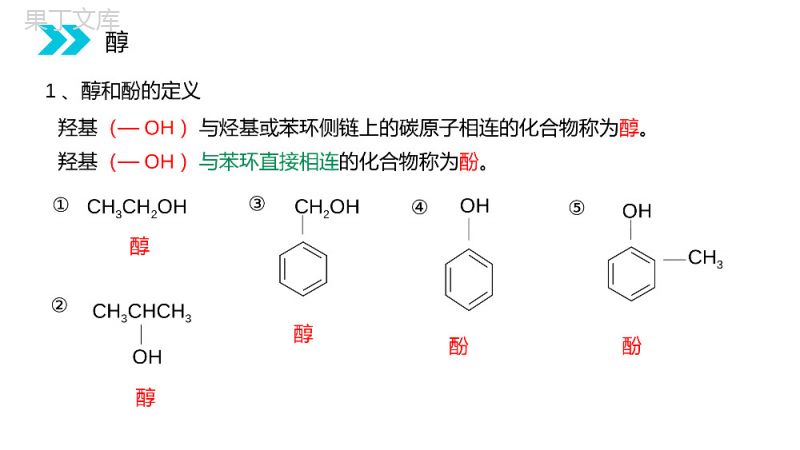
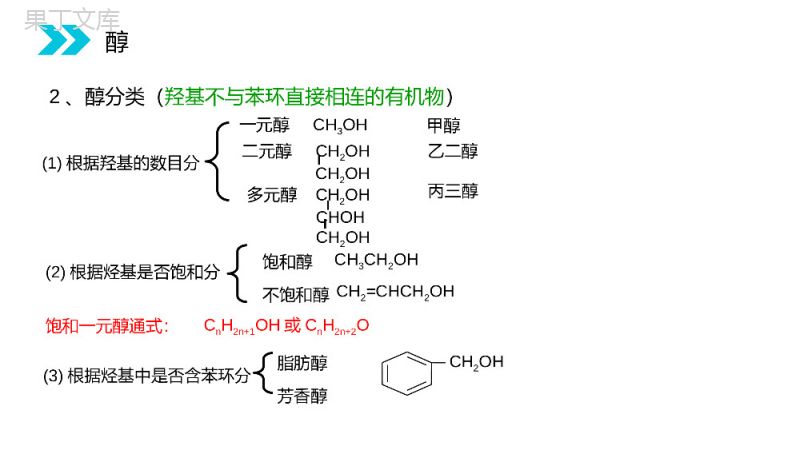
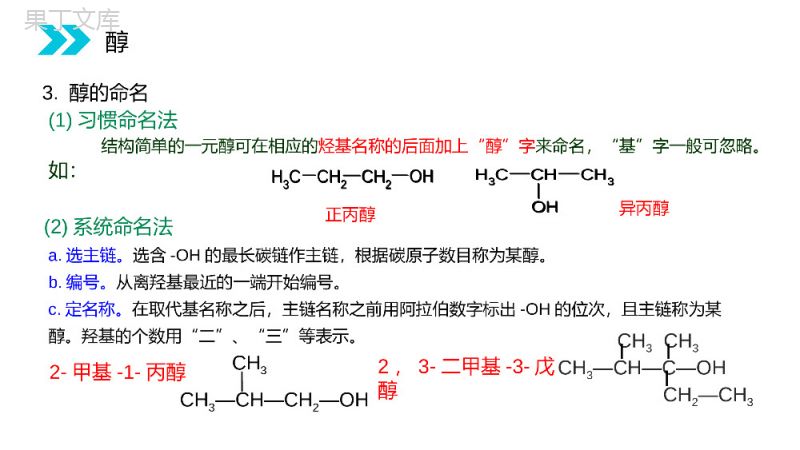
讲解人:办公资源时间:2020.6.1MENTALHEALTHCOUNSELINGPPT3.1.1醇第3章烃的含氧衍生物人教版高中选修五化学课件.问题1:醉酒的人为什么会脸红?问题2:如何检测酒驾?喝酒脸红的原因是什么呢?很多人以为是酒精导致的,其实不然,是乙醛引起的。乙醛具有让毛细血管扩张的功能,而脸部毛细血管的扩张才是脸部变红的原因。所以喝酒脸红的人意味着能迅速将乙醇转化成为乙醛。为了你我安全,开车不饮酒,饮酒不开车!新知导入羟基(—OH)与烃基或苯环侧链上的碳原子相连的化合物称为醇。羟基(—OH)与苯环直接相连的化合物称为酚。醇醇酚醇OHCH3CH2OHCH3CHCH3OHCH2OHOHCH3酚①②③④⑤1、醇和酚的定义醇(1)根据羟基的数目分一元醇CH3OH甲醇二元醇CH2OHCH2OH乙二醇多元醇CH2OHCHOHCH2OH丙三醇(2)根据烃基是否饱和分饱和醇不饱和醇(3)根据烃基中是否含苯环分脂肪醇芳香醇饱和一元醇通式:CnH2n+1OH或CnH2n+2OCH2OHCH3CH2OHCH2=CHCH2OH2、醇分类(羟基不与苯环直接相连的有机物)醇a.选主链。选含-OH的最长碳链作主链,根据碳原子数目称为某醇。b.编号。从离羟基最近的一端开始编号。c.定名称。在取代基名称之后,主链名称之前用阿拉伯数字标出-OH的位次,且主链称为某醇。羟基的个数用“二”、“三”等表示。CH3—CH—CH2—OHCH32-甲基-1-丙醇CH3—CH—C—OHCH3CH2—CH3CH32,3-二甲基-3-戊醇(2)系统命名法(1)习惯命名法结构简单的一元醇可在相应的烃基名称的后面加上“醇”字来命名,“基”字一般可忽略。如:OHCH3CH2CH2CH3CH3CHOH正丙醇异丙醇3.醇的命名醇OHCH3CH2CH2CH3CH3CHOHCH3CHCH2CH2CHCH3CH2CH3OH5-甲基-2-庚醇CH2CHCH2OHCH23-丁烯-1-醇CH2OHCH2OHCHOH1,2,3-丙三醇(或甘油、丙三醇)CH3CHCCH3OHOHCH32-甲基-2,3-丁二醇1、写出下列醇的名称醇醇类的同分异构体可有:(1)碳链异构、(2)羟基的位置异构,(3)相同碳原子数的饱和一元醇和醚是官能团异构4、醇的同分异构体4.醇的同分异构体书写1、写出C4H10O的所有同分异构体2、写出C4H8O的所有同分异构体醇5、几种重要的醇(3)乙二醇:无色、黏稠、有甜味的液体,它的水溶液凝固点_____________,可作为内燃机的__________(1)甲醇:最初是由木材干馏得到的,因此又称为___________,有酒精味,但___________。人饮用10mL,就能使眼睛失明,再多则能致死。(2)丙三醇俗称_____________,有护肤作用,是利用它具有___________性。木精有毒甘油亲水很低抗冻剂醇名称相对分子质量沸点/℃甲醇3264.7乙烷30-88.6乙醇4678.5丙烷44-42.1丙醇6097.2丁烷58-0.5表3-1相对分子质量相近的醇与烷烃的沸点比较6.醇的重要物理性质结论:相对分子质量相近的醇比烷烃的沸点高得多。因为醇分子间可以形成氢键。HHOOHHHOC2H5醇名称分子中羟基的数目沸点/0C乙醇178.5乙二醇2197.31—丙醇197.21、2—丙二醇21881、2、3—丙三醇3259P49表3-2一些醇的沸点请你仔细阅读表格的数据并作出解释。结论:由于羟基数目增多,使得分子间形成的氢键增多增强,熔沸点升高。醇1.沸点(1)因醇分子之间有氢键,沸点远高于相对分子质量相近的烷烃。(2)饱和一元醇随C数增加,醇的沸点升高。(3)相同碳原子数,羟基数目越多,分子间形成的氢键增多增强,沸点越高。2.水溶性(1)低级醇(如甲、乙、丙醇)与水任意比混溶。(2)随C数的增加,水溶性逐渐降低。(憎水基增大,削弱亲水基羟基的作用)醇的重要物理性质醇1.乙醇的结构C2H6OH—C—C—O—HHHHHCH3CH2OH或C2H5OH—OH(羟基)分子式结构式结构简式官能团O—HC—O键的极性较大,易断键二、乙醇颜色:气味:状态:沸点:密度:溶解性:无色透明特殊香味液体0.78g/ml比水小78℃,易挥发跟水以任意比互溶,本身良好的有机溶剂2、乙醇的物理性质检验C2H5OH(H2O)。除杂C2H5OH(H2O)。CuSO4先加CaO后蒸馏二、乙醇官能团是−OH,由于O吸引电子能力比C、H强,C−O键、O−H键均有较强极性,易断裂。3、化学性质H−C−C−O−HHHHH②①⑤③④结构决定性质二、乙醇3、乙醇的化学性质1、与金属Na的取代2CH3CH2OH+2Na→2CH3CH2ONa+H2↑小结:①活泼金属:K/Ca/Na/Mg/Al②乙醇与金属钠反应不如水与金属钠反应剧烈;羟基上的H原子的活泼性小于水分子中H原子1)取代反应2−OH~H2(断①)二、乙醇2R-OH+2Na→CH2CH2CH2+2Na→OHOH2R-ONa+H2↑CH2CH2CH2+H2↑ONaONa醇中羟基数判断:n(醇):n(H2)=21∶一元醇11∶二元醇23∶三元醇2−OH~H2二、乙醇醇取代反应(2)分子间脱水成醚(3)与HX反应(4)酯化反应C2H5−OH+HO−C2H5C2H5−O−C2H5+H2O浓H2SO4140℃C2H5−OH+H−BrC2H5−Br+H2O∆OCH3−C−OH+H−OC2H5CH3COOC2H5+H2O浓H2SO4∆(断①②)(断②)(断①)酸脱羟基,醇脱氢二、乙醇2)消去反应与−OH相连C的邻位C上有H,可脱H2O消去。CH2−CH2CH2=CH2↑+H2O浓H2SO4170℃HOHCH3OH−CH2OHCH3−C−CH2OHCH3CH3分子内脱水(断②⑤)结论:乙醇在不同温度下(140℃、170℃)生成不同的产物二、乙醇2)消去反应CH2CH2CH2=CH2↑+H2OHOH浓H2SO4170℃——常用于实验室制备乙烯①液液加热需注意什么?放入几片碎瓷片防止暴沸②浓硫酸的作用是什么?催化剂和脱水剂③为何使液体温度迅速升到170℃?140℃会发生副反应,生成乙醚二、乙醇④温度计的位置?温度计水银球要置于反应物的中央位置,因为需要测量的是反应物的温度。⑤混合液颜色为什么会呈现黑色?为什么?浓硫酸将无水酒精氧化生成碳的单质等多种物质,碳的单质使烧瓶内的液体带上了黑色。⑥实验中,溴水或高锰酸钾溶液颜色褪去,有何杂质气体干扰?如何除去?由于无水酒精和浓硫酸发生的氧化还原反应,反应制得的乙烯中往往混有H2O、CO2、SO2等气体。可将气体通过NaOH溶液。⑦为何用排水集气法收集?因为乙烯难溶于水,密度比空气密度略小。二、乙醇R-CH=CH2+H2OR-CH2CH2OHΔ浓硫酸浓硫酸ΔCH3CHCH2CH3OH|CH2=CHCH2CH3+H2O或CH3CH=CHCH3+H2O能进行消去反应吗?CH3—C—CH2—OHCH3CH3拓展:小结:跟羟基连接的C相邻的C上无H则不能发生消去反应是不是所有的醇都能发生消去反应?二、乙醇CH3CH2BrCH3CH2OH消去条件有β-H反应条件NaOH醇溶液、加热浓H2SO4、170℃化学键的断裂C−Br、C−HC−O、C−H化学键的生成C=CC=C反应产物CH2=CH2、HBrCH2=CH2、H2O(教材P50)溴乙烷与乙醇都能发生消去反应,它们有什么异同?二、乙醇3)氧化反应①燃烧(淡蓝色火焰,放出大量热)②能使酸性高锰酸钾溶液褪色(全断键)CH3CH2OHCH3COOHKMnO4(H+,aq)或K2Cr2O7(H+,aq)二、乙醇【分组实验】实验步骤及现象引导:(1)在锥形瓶中加入2mL无水乙醇;(3)趁热将铜丝浸入锥形瓶里的乙醇中;观察铜丝颜色的变化(4)反复多次。注意乙醇的气味变化铜丝在酒精灯上灼烧后,铜丝由红变黑。发现铜丝又由黑变红。闻到有刺激性气味。(2)将铜丝在酒精灯上灼烧;观察铜丝颜色的变化2Cu+O22CuO△二、乙醇乙醛2Cu+O22CuOHHHOCHHHC+O2CHHHCOH22+2H2O催化剂乙醛1.铜在整个过程中起什么作用?2.乙醇分子中有哪些化学键断裂?又生成了哪些化学键?2CuO+2CH3CH2OH2Cu+2CH3CHO+2H2O2CH3CH2OH+O22CH3CHO+2H2OCu分析:总③催化氧化二、乙醇HHHOCHHHC+O2CHHHCOH22+2H2O叔醇(连接—OH的叔碳原子上没有H),则不能去氢氧化。COHR2R1R3(3).(2).2CH—OH+O2R2R1Cu△(1).2R—CH2—OH+O2Cu△连接-OH的碳原子上必须有H,才发生去氢氧化(催化氧化)伯醇(—OH在伯碳——首位碳上),去氢氧化为醛O=2R—C—H+2H2O仲醇(—OH在仲碳-中间碳上),去氢氧化为酮O=2R1—C—R2+2H2O二、乙醇1.下列醇不能在铜的催化下发生氧化反应的是()A.B.CH3CH2CH2OHC.D.D二、乙醇2.下列各物质中,能被铜催化氧化,且产物为醛的是(双选)()BD二、乙醇被强氧化剂KMnO4或K2Cr2O7氧化实验现象:紫色褪去溶液或由橙黄色变为绿色CH3CH2OHCH3CHOCH3COOH氧化氧化乙醇乙醛乙酸K2Cr2O7或KMnO4K2Cr2O7或KMnO4二、乙醇事故调查显示:大约50%-60%的交通事故与酒后驾驶有关。K2Cr2O7Cr2(SO4)3(橙黄色)(蓝绿色)交警判断驾驶员是否酒后驾车的方法C2H5OH二、乙醇1、如何检验生成的气体是乙烯?因为乙醇也能使酸性高锰酸钾溶液褪色,干扰乙烯气体的检验。先通水除去反应时挥发出的乙醇CH2-CH2HBr醇△+NaOHCH2=CH2↑+NaBr+H2O二、乙醇醇的氧化规律醇能否被氧化以及被氧化的产物的类别,取决于与羟基相连的C上H的个数。R−CH2OHR1−CH−R2OH2~3个H伯醇1个H仲醇无H叔醇R1−C−R2OHR3R−CHOR−COOHKMnO4(H+)或K2Cr2O7(H+)Cu、O2∆KMnO4(H+)或K2Cr2O7(H+)Cu、O2∆R1−C−R2O不可被催化氧化课堂总结②①⑤③④H―C―C―O―HHHHH反应断键位置分子间脱水与HX反应②④②①③①②与金属反应消去反应催化氧化①醇的反应情况课堂总结醇卤代烃醛或酮醇钠醚酯烯烃氧气金属钠氢卤酸羧酸浓硫酸浓硫酸课堂总结1.乙醇分子结构中各种化学键如图所示,关于乙醇在各种反应中断裂键的说法中,不正确的是()A.与金属钠反应时键①断裂B.和浓H2SO4共热到170℃时,键②与键⑤断裂C.和浓H2SO4共热到140℃时,仅有键②断裂D.在铜催化下与O2反应时,键①和键③断裂CH−C−C−O−HHHHH②①⑤③④课堂练习2.下列物质既能发生消去反应生成相应的烯烃又能被氧化成相应的醛的是()A.CH3OHB.CH2(OH)CH2CH3C.CH3CH(OH)CH3D.(CH3)3COHB课堂练习感谢您下载68素材平台上提供的PPT作品,为了您和68素材以及原创作者的利益,请勿复制、传播、销售;素材均来源于网络用户分享,故68素材不具备充分的监控能力来审查图片是否存在侵权等情节。68素材不拥有此类图片的版权,本站所有资源仅供学习与交流,不得用于任何商业用途的范围,用户应自觉遵守著作权法及其他相关法律的规定,不得侵犯本网站及权利人的合法权利,给68素材和任何第三方造成损失的,侵权用户应负全部责任。版权声明1.完成教材P55习题1、22、完成补充作业3、预习下一节内容苯酚作业布置讲解人:办公资源时间:2020.6.1MENTALHEALTHCOUNSELINGPPT感谢各位的聆听第3章烃的含氧衍生物人教版高中选修五化学课件.
提供《醇》人教版高二化学选修五PPT课件(第3.1.1课时).pptx会员下载,编号:1701021399,格式为 xlsx,文件大小为39页,请使用软件:wps,office Excel 进行编辑,PPT模板中文字,图片,动画效果均可修改,PPT模板下载后图片无水印,更多精品PPT素材下载尽在某某PPT网。所有作品均是用户自行上传分享并拥有版权或使用权,仅供网友学习交流,未经上传用户书面授权,请勿作他用。若您的权利被侵害,请联系963098962@qq.com进行删除处理。

 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载