肉桂酸的制备(完整版),肉桂酸的制备实验报告
本作品内容为肉桂酸的制备(完整版),格式为 docx ,大小 89989 KB ,页数为 4页
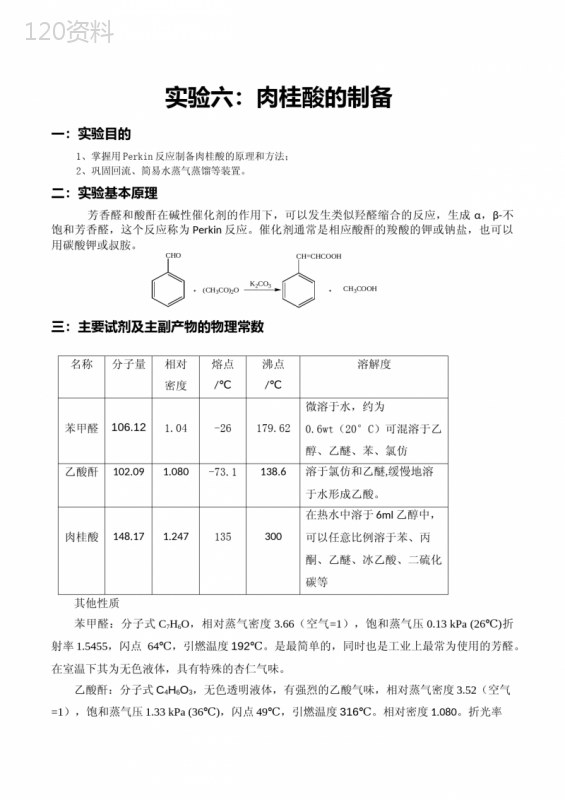
('实验六:肉桂酸的制备一:实验目的1、掌握用Perkin反应制备肉桂酸的原理和方法;2、巩固回流、简易水蒸气蒸馏等装置。二:实验基本原理芳香醛和酸酐在碱性催化剂的作用下,可以发生类似羟醛缩合的反应,生成α,β-不饱和芳香醛,这个反应称为Perkin反应。催化剂通常是相应酸酐的羧酸的钾或钠盐,也可以用碳酸钾或叔胺。CHO(CH3CO)2OCH=CHCOOHCH3COOHK2CO3三:主要试剂及主副产物的物理常数名称分子量相对密度熔点/℃沸点/℃溶解度苯甲醛106.121.04-26179.62微溶于水,约为0.6wt(20°C)可混溶于乙醇、乙醚、苯、氯仿乙酸酐102.091.080-73.1138.6溶于氯仿和乙醚,缓慢地溶于水形成乙酸。肉桂酸148.171.247135300在热水中溶于6ml乙醇中,可以任意比例溶于苯、丙酮、乙醚、冰乙酸、二硫化碳等其他性质苯甲醛:分子式C7H6O,相对蒸气密度3.66(空气=1),饱和蒸气压0.13kPa(26)℃折射率1.5455,闪点64℃,引燃温度192℃。是最简单的,同时也是工业上最常为使用的芳醛。在室温下其为无色液体,具有特殊的杏仁气味。乙酸酐:分子式C4H6O3,无色透明液体,有强烈的乙酸气味,相对蒸气密度3.52(空气=1),饱和蒸气压1.33kPa(36)℃,闪点49℃,引燃温度316℃。相对密度1.080。折光率1.3904。低毒,半数致死量(大鼠,经口)1780mG/kG。有腐蚀性。勿接触皮肤或眼睛,以防引起损伤。有催泪性。易燃,其蒸气与空气可形成爆炸性混合物,遇明火、高热能引起燃烧爆炸。与强氧化剂接触可发生化学反应。肉桂酸:分子式C9H8O2,又名β-苯丙烯酸,有顺式和反式两种异构体。通常以反式形式存在,为白色单斜晶体,微有桂皮气味。肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料。四:主要试剂规格及用量名称规格用量物质的量苯甲醛新蒸(11.25g)3.8mL0.0375mol乙酸酐新蒸(3.98g)10.5mL约0.111mol碳酸钾无水5.25g——氢氧化钠10%30mL——浓盐酸1:130mL——水-乙醇溶液3:1————五:实验装置图主要仪器:100mL圆底烧瓶,球形冷凝管,直形冷凝管,温度计,简易水蒸气蒸馏装置,抽滤装置,250mL烧杯,表面皿。六:实验简单操作步骤及实验现象记录实验步骤实验现象分别量取3.8mL新蒸馏过的苯甲醛和10.5mL新蒸馏过的乙酸酐于100mL干燥的圆底烧瓶中,摇匀,再加入无明显现象,白色固体不溶解5.25g研碎无水碳酸钾将烧瓶置于石棉网上方1~2cm,使反应物保持微微沸腾,刚好有回流,回流45分钟刚开始加热时,液体变成乳白色且有白色气泡冒出,随着加热时间加长,溶液颜色变橘红色,且有少量固体出现。反应结束,稍冷,趁还没有出现固体,迅速转入长颈圆底烧瓶(水蒸气蒸馏用)中,用约30mL热水分几次冲洗反应瓶洗液一并转入长颈圆底烧瓶。用玻璃棒轻轻捣碎固体后进行水蒸气蒸馏,至无油状物蒸出为止加热一段时间后,长颈烧瓶内液体剧烈翻滚,蒸出白色乳浊液。蒸馏大约50分钟后,用表面皿承接少量蒸出的液体,发现表面没有少量油状物了。将长颈圆底烧瓶中的剩余物转入一洁净的烧杯中,冷却溶液表层,内部有凝固物加入约30mL10%氢氧化钠溶液中和至溶液呈碱性,使生成的肉桂酸形成钠盐而溶解。固体溶解,溶液呈深橘红色再加入30mL水,并加入适量活性炭,煮沸5min,趁热过滤。滤液冷却后,用30mL1:1的盐酸酸化至酸性,冷却,待晶体全部析出后抽滤,用10mL冷水分两次洗涤沉淀,抽干后。粗产品在80℃烘箱中烘干[2]。产率约3g。可用3:1的水-乙醇溶液进行重结晶。滴加HCL酸化时,产生白色糊状物,经抽滤后,得到纯白色物质。烘干得到5.5g灰白色粉末状物质七:实验结果及分析本次实验得到5.5g灰白色产物,而纯的肉桂酸应该纯白色的,说明本次实验过程中的有的操作是不规范的。可能有一下几点原因:1、加入活性炭煮沸后,使用的烧杯没有洗干净,而我在之后的步骤里都再次用到了该烧杯;2、加活性炭煮沸并趁热过滤时,可能没有过滤完全。计算产率:生成的肉桂酸理论值:m:0.0375mol148.17g/mol=5.56g生成的肉桂酸实际值:m:5.5g产率:本实验产率较高可能原因:产品烘干不够完全。八:思考题1、本实验需要注意的地方:1、加热的温度最好用油浴,控温在160—1800C,若用电炉加热,必须使烧瓶底离开电炉4~5cm,电炉开小些,慢慢加热到回流状态,等于用空气浴进行加热。如果紧挨着电炉,会因温度太高,反应太激烈,结果形成大量树脂状物质,甚至使肉桂酸一无所有,这点是实验的关键。2、反应刚开始,会因二氧化碳的放出而有大量泡沫产生,这时候加热温度尽量低些,等到二氧化碳大部分出去后,再小心加热到回流态,这时溶液呈浅棕黄色。反应结束的标志是反应时间已到规定时间,有小量固体出现。反应结束后,再加热水,可能会出现整块固体,很不好压碎,干脆不要去压碎它(当然能搞碎是最好的),以免触碎反应瓶。等水汽蒸馏时,温度一高,它会溶解的。2、用水蒸气蒸馏能除去什么?能不能不用水蒸气蒸馏?如何判断蒸馏终点?答:①除去未反应的苯甲醛;②不行,必须用水蒸气蒸馏,因为混合物中含有大量的焦油状物质,通常的蒸馏、过滤、萃取等方法都不适用;③当流出液澄清透明不再含有有机物质的油滴时,即可断定水蒸汽蒸馏结束(也可用盛有少量清水的锥形瓶或烧杯来检查是否有油珠存在)。3、什么情况下需要采用水蒸汽蒸馏?答:下列情况需要采用水蒸气蒸馏:(1)混合物中含有大量的固体,通常的蒸馏、过滤、萃取等方法都不适用。(2)混合物中含有焦油状物质,采用通常的蒸馏、萃取等方法都不适用。(3)在常压下蒸馏会发生分解的高沸点有机物质。4、怎样正确进行水蒸汽蒸馏操作?答:(1)在进行水蒸气蒸馏之前,应认真检查水蒸气蒸馏装置是否严密。(2)开始蒸馏时,应将T形管的止水夹打开,当水蒸气发生器里的水沸腾,有大量水蒸气溢出时再旋紧夹子,使水蒸气进入三颈烧瓶中,并调整加热速度,以馏出速度2—3滴/秒为宜。(3)操作中要随时注意安全管中的水柱是否有异常现象发生,若有,应立即打开夹子,停止加热,找出原因,排除故障后方可继续加热。',)
提供肉桂酸的制备(完整版),肉桂酸的制备实验报告会员下载,编号:1700760935,格式为 docx,文件大小为4页,请使用软件:wps,office word 进行编辑,PPT模板中文字,图片,动画效果均可修改,PPT模板下载后图片无水印,更多精品PPT素材下载尽在某某PPT网。所有作品均是用户自行上传分享并拥有版权或使用权,仅供网友学习交流,未经上传用户书面授权,请勿作他用。若您的权利被侵害,请联系963098962@qq.com进行删除处理。

 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载