《化学平衡》人教版高二化学选修4PPT课件(第3课时).pptx


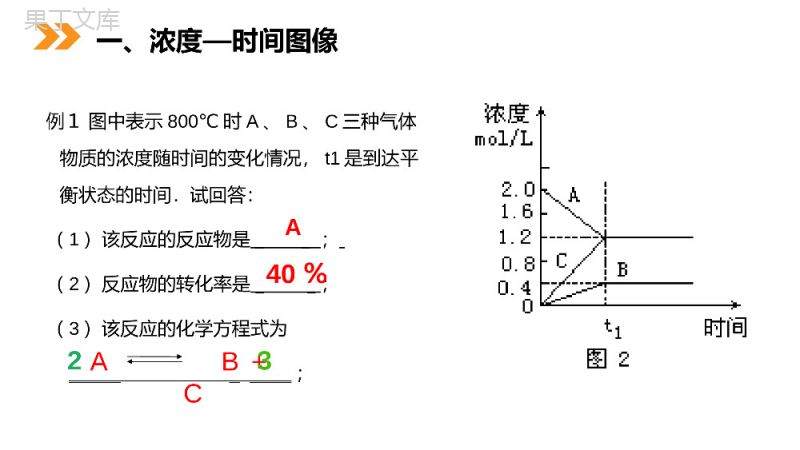
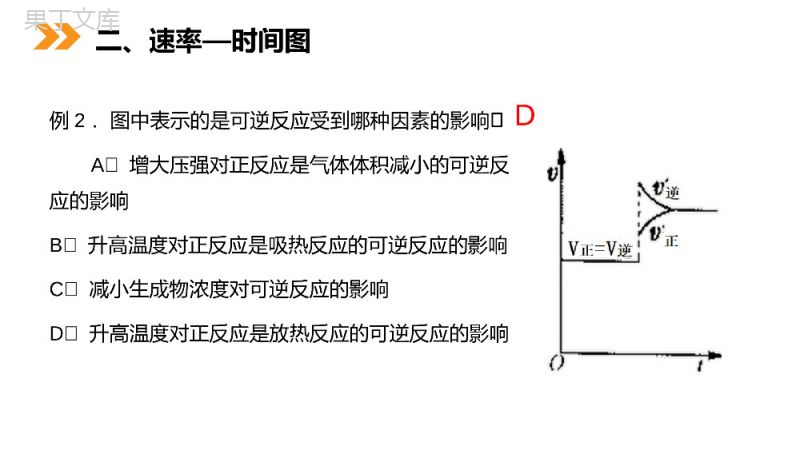
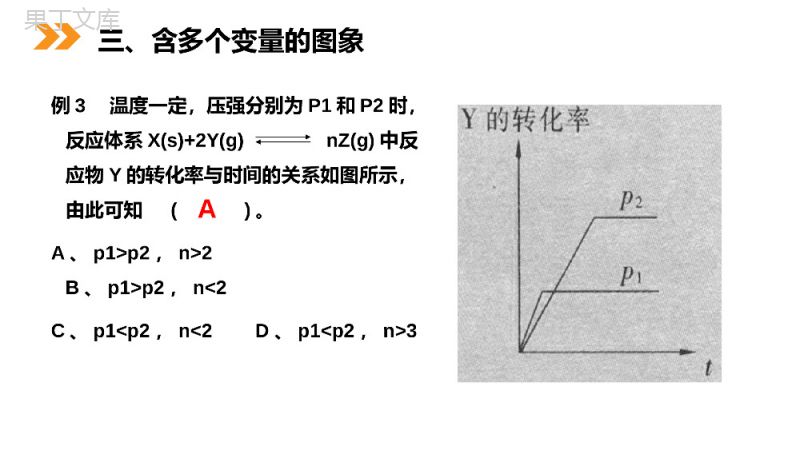
第3课时化学平衡图像MENTALHEALTHCOUNSELINGPPT第3节化学平衡第二章化学反应速率和化学平衡人教版高中化学选修4(高二)可逆反应:mA(g)+nB(g)pC(g)+qD(g)在一定条件下建立平衡时,V正=V逆、c(A)、c(B)、c(C)、c(D)保持不变。当外界条件改变时:V正、V逆会发生变化,变化后,若V正=V逆时,平衡不移动;若V正>V逆时,平衡向右移动;若V正<V逆时,平衡向左移动。通过比较新的V正、V逆的相对大小,便可确定化学平衡移动的方向。复习例1图中表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间.试回答:(1)该反应的反应物是__;(2)反应物的转化率是__;(3)该反应的化学方程式为__________;A40%AB+C23一、浓度—时间图像例2.图中表示的是可逆反应受到哪种因素的影响A增大压强对正反应是气体体积减小的可逆反应的影响B升高温度对正反应是吸热反应的可逆反应的影响C减小生成物浓度对可逆反应的影响D升高温度对正反应是放热反应的可逆反应的影响D二、速率—时间图例3温度一定,压强分别为P1和P2时,反应体系X(s)+2Y(g)nZ(g)中反应物Y的转化率与时间的关系如图所示,由此可知()。A、p1>p2,n>2B、p1>p2,n<2C、p1
提供《化学平衡》人教版高二化学选修4PPT课件(第3课时).pptx会员下载,编号:1701021388,格式为 xlsx,文件大小为20页,请使用软件:wps,office Excel 进行编辑,PPT模板中文字,图片,动画效果均可修改,PPT模板下载后图片无水印,更多精品PPT素材下载尽在某某PPT网。所有作品均是用户自行上传分享并拥有版权或使用权,仅供网友学习交流,未经上传用户书面授权,请勿作他用。若您的权利被侵害,请联系963098962@qq.com进行删除处理。

 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载