《常见的酸和碱》(第2课时常见的碱)2021-2022学年九年级化学人教版下册




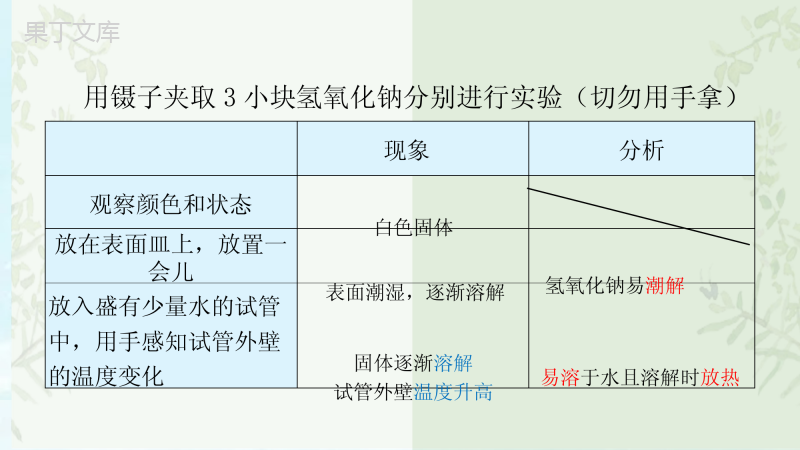
课题1常见的碱人教版九年级化学常见的酸和碱第二课时常见的碱名称角度从名称上来看一般叫.氢氧化某组成角度从组成上看都含离子氢氧根性质角度从性质上看碱溶液都呈性碱氢氧化钙氢氧化钠氢氧化铝氢氧化钾KOH知识精讲(1)NaOH:有很强的腐蚀性,俗称烧碱、火碱、苛性钠NaOH(2)不慎将氢氧化钠溶液沾到皮肤上,立即用大量水冲洗,然后再涂上硼酸溶液。一、常见的碱1、氢氧化钠的性质知识精讲现象分析观察颜色和状态放在表面皿上,放置一会儿放入盛有少量水的试管中,用手感知试管外壁的温度变化用镊子夹取3小块氢氧化钠分别进行实验(切勿用手拿)白色固体表面潮湿,逐渐溶解氢氧化钠易潮解固体逐渐溶解试管外壁温度升高易溶于水且溶解时放热1、氢氧化钠的性质(3)暴露在空气中易吸收水分,表面潮湿并逐渐溶解,这种现象叫做潮解,氢氧化钠固体溶解时放热。在空气中放置后的氢氧化钠新制的氢氧化钠(4)实验室用途:①做干燥剂可干燥:H2、O2、NH3等中性和碱性气体不可干燥:CO2、HCl等酸性气体干燥管干燥装置总结液体干燥剂固体干燥剂如:浓硫酸,具有吸水性.如:氢氧化钠、氧化钙固体具有吸水性。(碱石灰)知识精讲(5)化工原料肥皂石油印染造纸油污清洁2.氢氧化钙[Ca(OH)2](3)制取:CaO+H2O=Ca(OH)2(CaO可做食品干燥剂的原因)(4)用途:①做建筑材料:砌砖、刷墙(石灰浆变硬是化学变化);②保护树木,防止冻伤和害虫生卵;③和硫酸铜混合配制农药波尔多液;④改良酸性土壤;(2)物理性质:白色粉末,微溶于水,水溶液俗称石灰水。当石灰水中有较多未溶解的氢氧化钙时,称石灰乳或石灰浆。(1)俗称:熟石灰或消石灰俗称苛性钠、火碱、烧碱(强腐蚀性)熟石灰、消石灰(有腐蚀性)颜色、状态白色固体白色粉末溶解性极易溶于水,放出大量热微溶于水(溶液俗称石灰水)其他易潮解(作干燥剂)可由生石灰加水制得(放热)CaO+H2O=Ca(OH)2用途化工原料:广泛用于肥皂、石油、造纸、纺织、印染等工业。砌砖、抹墙;制氢氧化钠、制漂白粉;降低土壤酸性;制波尔多液。氢氧化钠和氢氧化钙的物理性质和用途物质性质氢氧化钠氢氧化钙可溶性碱氢氧化钾KOH氢氧化钠NaOH氨水NH3.H2O氢氧化钙Ca(OH)2氢氧化钡Ba(OH)2Cu(OH)2氢氧化铜Mg(OH)2氢氧化镁Fe(OH)3氢氧化铁Al(OH)3氢氧化铝难溶性碱不能使指示剂变色可溶性碱有五位钾钠氨钙钡碱的分类蓝色红褐色二、可溶性碱的化学性质1.碱溶液能使紫色的石蕊溶液变蓝色,使无色的酚酞溶液变红色。回忆检验二氧化碳的方法,并写出化学方程式Ca(OH)2+CO2=CaCO3↓+H2O思考:氢氧化钠能否与二氧化碳反应?如何设计实验方案2.碱溶液能与某些非金属氧化物(主要是CO2、SO2,不包含CO)反应2NaOH+CO2=Na2CO3+H2O(吸收CO2)Ca(OH)2+CO2=CaCO3↓+H2O(检验CO2)氢氧化钠、氢氧化钙放置在空气中会发生变质,所以氢氧化钠必须密封保存。碱+非金属氧化物→盐+H2O2NaOH+SO2=Na2SO3+H2OCa(OH)2+SO2=CaSO3+H2O(1)碱溶液与CO2反应(2)碱溶液与SO2反应3、碱+酸→盐+水练习:分别写出氢氧化铁、氢氧化钙和盐酸、硫酸的反应Ca(OH)2+2HCl==CaCl2+2H2OFe(OH)3+3HCl==FeCl3+3H2O2Fe(OH)3+3H2SO4==Fe2(SO4)3+6H2O如:NaOH+HCl==NaCl+H2O;2NaOH+H2SO4==Na2SO4+2H2O;红褐色固体溶解,溶液变成黄色红褐色固体溶解,溶液变成黄色4、碱+盐→新碱+新盐2NaOH+CuCl2=3NaOH+FeCl3=Cu(OH)2↓+2NaClFe(OH)3↓+3NaCl有蓝色沉淀出现有红褐色沉淀出现化合反应分解反应置换反应定义类型特征由两种或两种以上物质生成另一种物质的反应由一种物质生成两种或两种以上其它物质的反应由一种单质与一种化合物反应,生成另一种单质与另一种化合物的反应A+B→ABAB→A+B+….AB+C→A+BC反应物为多种而生成物只有一种,即“多变一”反应物只有一种而生成物有多种,即“一变多”反应物与生成物都是两种,且都是单质和化合物化学基本反应类型知识精讲1、酸能与金属氧化物反应,盐和水。Fe2O3+6HCl===2FeCl3+3H2OFe2O3+3H2SO4===Fe2(SO4)3+3H2O2、酸能与碱反应,生成盐和水。NaOH+HCl===NaCl+H2OCa(OH)2+2HCl===CaCl2+2H2O3、酸能与某些盐反应。CaCO3+2HCl===CaCl2+H2O+CO2↑Na2CO3+2HCl===2NaCl+H2O+CO2↑4、碱+盐→新碱+新盐2NaOH+CuCl2=3NaOH+FeCl3=Cu(OH)2↓+2NaClFe(OH)3↓+3NaCl复分解反应1.定义:在溶液中,由两种化合物相互交换成分,生成另外两种化合物的反应。2.表达式:AB+CD→AD+CB3.发生条件:生成物中有沉淀或有气体或有水生成。特点:双交换、价不变、首尾连(双选)下列反应中不属于复分解反应的是()A.H2SO4+Ca(OH)2CaSO4+2H2OB.H2SO4+BaCl2BaSO4↓+2HClC.2HCl+FeFeCl2+H2↑D.2HCl+CaCO3CaCl2+H2O+CO2↑CEE.CO2+2NaOH====Na2CO3+H2O无交换A.H2SO4+Ca(OH)2CaSO4+2H2OB.H2SO4+BaCl2BaSO4↓+2HClC.2HCl+FeFeCl2+H2↑D.2HCl+CaCO3CaCl2+H2O+CO2↑硝酸盐,全可溶盐酸盐,银不溶(AgCl白色沉淀)硫酸盐,钡不溶(BaSO4白色沉淀)碳酸盐,可溶只有钾、钠盐,不溶都是白沉淀Cu(OH)2氢氧化铜蓝色红褐色Fe(OH)3氢氧化铁Mg(OH)2白色氢氧化镁氢氧化铝Al((OH)3白色判断下列物质是否溶于水:Na2CO3AgClBaCO3MgSO4BaSO4Cu(OH)2Fe(OH)3Ba(OH)2Mg(OH)2AgNO3NaNO3不溶溶溶溶溶不溶不溶不溶不溶溶不溶答案练习:(1)氢氧化钠和氯化铜的反应(2)氢氧化钠和氯化铁的反应(3)BaCl2+H2SO4(4)BaCl2+NaOH(5)Na2CO3+NaOH复分解反应发生的条件:只有当两种化合物相互交换成分,①生成水;②生成气体;③生成沉淀。(满足一条即可)蒸馏水乙醇稀盐酸稀硫酸氢氧化钠溶液氢氧化钙溶液不导电不导电导电导电导电导电H+Cl-H2OH2OH2OC2H6OH+SO42-H2ONa+OH-H2OCa2+OH-H2OHCl→H++Cl-H2SO4→2H++SO42-NaOH→Na++OH-Ca(OH)2→Ca2++2OH-分子不能自由移动的离子1、在不同的酸溶液中都含有相同的H+,所以,酸有一些相似的性质。2、在不同的碱溶液中都含有相同的OH-,所以碱也有一些相似的性质。能自由移动的离子三、酸碱具有通性的原因
提供《常见的酸和碱》(第2课时常见的碱)2021-2022学年九年级化学人教版下册会员下载,编号:1701029056,格式为 xlsx,文件大小为26页,请使用软件:wps,office Excel 进行编辑,PPT模板中文字,图片,动画效果均可修改,PPT模板下载后图片无水印,更多精品PPT素材下载尽在某某PPT网。所有作品均是用户自行上传分享并拥有版权或使用权,仅供网友学习交流,未经上传用户书面授权,请勿作他用。若您的权利被侵害,请联系963098962@qq.com进行删除处理。

 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载