色散型红外光谱仪工作原理,色散型红外光谱仪的工作原理


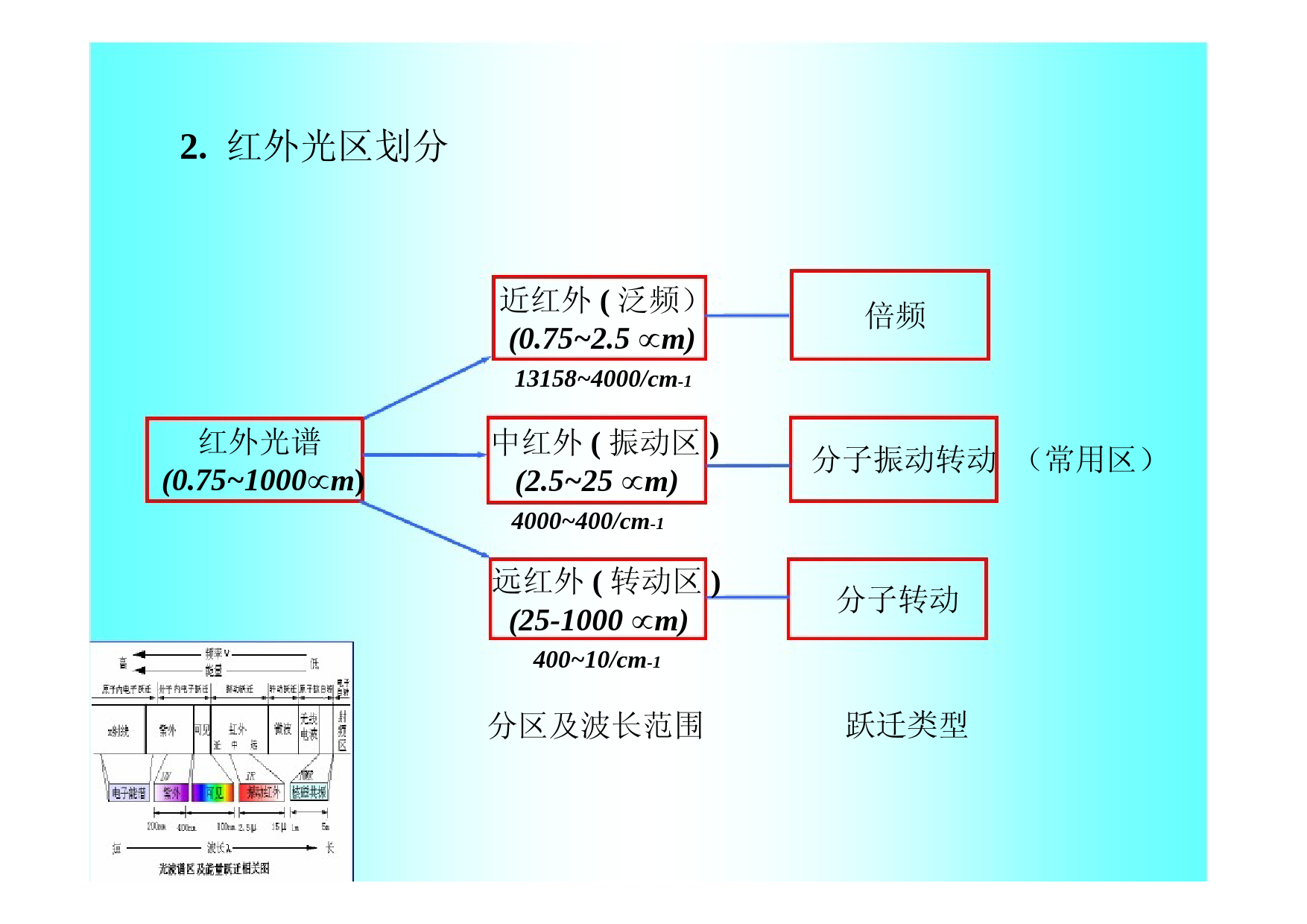


3.1概述1.定义:红外光谱又称分子振动转动光谱,属分子吸收光谱。样品受到频率连续变化的红外光照射时,分子吸收其中一些频率的辐射,分子振动或转动引起偶极矩的净变化,使振-转能级从基态跃迁到激发态,相应于这些区域的透射光强减弱,记录百分透过率T%对波数或波长的曲线,即为红外光谱。主要用于化合物鉴定及分子结构表征,亦可用于定量分析。2.红外光区划分红外光谱(0.75~1000m)倍频分子振动转动(常用区)分子转动跃迁类型近红外(泛频)(0.75~2.5m)13158~4000/cm-1中红外(振动区)(2.5~25m)4000~400/cm-1远红外(转动区)(25-1000m)400~10/cm-1分区及波长范围3.红外光谱的作用分子结构的基础研究:测定分子的键长、键角以推算出分子的立体构型;据所得的力常数知道化学键的强弱;用于化学组成的分析:最常用,据光谱中吸收峰的位置和形状来推断未知物结构、据特征吸收峰的强度来测定混合物中各组分的含量。1)确定官能团2)确定化合物的类别(芳香类)3)推测分子结构(简单化合物)4)定量分析4.红外光谱特点1)红外吸收只有振-转跃迁,能量低;2)应用范围广:除单原子分子及单核分子外,几乎所有有机物均有红外吸收;3)分子结构更为精细的表征:通过IR谱的波数位置、波峰数目及强度确定分子基团、分子结构;4)固、液、气态样均可用,且用量少、不破坏样品;5)分析速度快。6)与色谱等联用(GC-FTIR)具有强大的定性功能。IRUV起源分子振动能级伴随转动能级跃迁分子外层价电子能级跃迁适用所有红外吸收的化合物具n-π跃迁有机化合物具π-π跃迁有机化合物特征性特征性强简单、特征性不强用途定量推测有机化合物共轭骨架鉴定化合物类别鉴定官能团推测结构IR与UV的区别3.2基本原理1.产生红外吸收的条件分子吸收辐射产生振转跃迁必须满足两个条件:条件一:辐射光子的能量应与振动跃迁所需能量相等。根据量子力学原理,分子振动能量Ev是量子化的,即EV=(V+1/2)hvv为分子振动频率,V为振动量子数,其值取0,1,2,…分子中不同振动能级差为△EV=△Vhv也就是说,只有当△EV=Ea或者va=△V·v时,才可能发生振转跃迁。例如当分子从基态(V=0)跃迁到第一激发态(V=1),此时△V=1,即va=v磁场条件二:辐射与物质之间必须有耦合作用电场交变磁场v分子固有振动va偶极矩变化(能级跃迁)耦合不耦合红外吸收无偶极矩变化无红外吸收对称分子:没有偶极矩,辐射不能引起共振,无红外活性。如:N2、O2、Cl2等。非对称分子:有偶极矩,红外活性。当一定频率的红外光照射分子时,若分子中某个基团的振动频率和它一样,二者就会产生共振,此时光的能量通过分子偶极距的变化而传递给分子,这个基团就会吸收一定频率的红外光,产生振动跃迁;若红外光的振动频率和分子中各基团的振动频率不符合,该部分的红外光就不会被吸收。若用连续改变频率的红外光照射某试样,由于该试样对不同频率的红外光的吸收与否,使通过试样后的红外光在一些波长范围内变弱(被吸收),在另一些范围内则不吸收。影响基本振动跃迁的波数或频率的直接因素为化学键力常数k和原子质量。k大,化学键的振动波数高;质量m大,化学键的振动波数低。经典力学导出的波数计算式为近似式,仅适用于双原子分子或多原子分子中影响小的谐振子。因为振动能量变化是量子化的,分子中各基团之间、化学键之间会相互影响,即分子振动的波数与分子结构(内因)和所处的化学环境(外因)有关。2)多原子分子多原子分子的振动更为复杂(原子多、化学键多、空间结构复杂),但可将其分解为多个简正振动来研究。简正振动整个分子质心不变、整体不转动、各原子在原地作简谐振动且频率及位相相同。此时分子中的任何振动可视为所有上述简谐振动的线性组合。简正振动基本形式伸缩振动ν:原子沿键轴方向伸缩,键长变化但键角不变的振动。变形振动δ:基团键角发生周期性变化,但键长不变的振动。又称弯曲振动或变角振动。下图给出了各种可能的振动形式(以甲基和亚甲基为例)。理论振动数(峰数)设分子的原子数为n,对非线型分子,理论振动数=3n-6如H2O分子,其振动数为3×3-6=3对线型分子,理论振动数=3n-5如CO2分子,其理论振动数为3×3-5=4非线型分子:n个原子一般有3n个自由度,但有3个平动和3个绕轴转动无能量变化;线型分子:n个原子一般有3n个自由度,但有3个平动和2个绕轴转动无能量变化。理论上,多原子分子的振动数应与谱峰数相同,但实际上,谱峰数常常少于理论计算出的振动数,这是因为:a)偶极矩的变化△μ=0的振动,不产生红外吸收,如CO2;b)谱线简并(振动形式不同,但其频率相同);c)仪器分辨率或灵敏度不够,有些谱峰观察不到。3.谱带强度分子对称度高,振动偶极矩小,产生的谱带就弱;反之则强。如C=C,C-C因对称度高,其振动峰强度小;而C=X,C-X,因对称性低,其振动峰强度就大。峰强度可用很强(vs)、强(s)、中(m)、弱(w)、很弱(vw)等来表示。说明:1)吸收峰强度与分子偶极距变化的平方成正比。而偶极距变化主要由化学键两端原子间的电负性差;振动形式;其它如共振、氢键、共轭等因素决定;2)强度比UV-Vis强度小2-3个数量级;3)IR光度计能量低,需用宽狭缝,同一物质的ε随不同仪器而不同,因此常用w,s,m等来表示吸收强度。4.振动频率1)基团频率通过对大量标准样品的红外光谱的研究,处于不同有机物分子的同一种官能团的振动频率变化不大,即具有明显的特征性。这是因为连接原子的主要为价键力,处于不同分子中的价键力受外界因素的影响有限!即各基团有其自已特征的吸收谱带。通常,基团频率位于4000~1300cm-1之间。可分为三个区。苯衍生物的红外光谱图单、双键伸缩振动(不含氢)1800-900C-O(1300-1000)C-(N、F、P),P-O,Si-O面内外弯曲振动900-650用于顺反式结构、取代类型的确定2)指纹区(可分为两个区)在红外分析中,通常一个基团有多个振动形式,同时产生多个谱峰(基团特征峰及指纹峰),各类峰之间相互依存、相互佐证。通过一系列的峰才能准确确定一个基团的存在。以上将中红外区分成四个区域,仅是企图将谱图稍加系统化以利于解释,而实际上关于识谱的程序至今并无一定规则。5.影响基团频率的因素基团频率主要由化学键的力常数决定。但分子结构和外部环境因素也对其频率有一定的影响。1)电子效应:引起化学键电子分布不均匀的效应。诱导效应(Inductioneffect):取代基电负性—静电诱导—电子分布改变—k增加—特征频率增加(移向高波数)。共轭效应(Conjugatedeffect):电子云密度均化—键长变长—k降低—特征频率减小(移向低波数)。中介效应(Mesomericeffect):孤对电子与多重键相连产生的p-π共轭,结果类似于共轭效应。当诱导与共轭两种效应同时存在时,振动频率的位移和程度取决于它们的净效应。a.诱导效应:吸电子基团使吸收峰向高频方向移动(蓝移)R-CORνC=01715cm-1;R-COHνC=01730cm-1;R-COClνC=01800cm-1;R-COFνC=01920cm-1;F-COFνC=01928cm-1;R-CONH2νC=01920cm-1b.共轭效应(红移)OCH3CCH3COCH3COCH3CO1715cm-11685cm-11685cm-11660cm-12)氢键效应(X-H)形成氢键使电子云密度平均化(缔合态),使体系能量下降,基团伸缩振动频率降低,其强度增加但峰形变宽。如羧酸RCOOH(νC=O=1760cm-1,νO-H=3550cm-1);(RCOOH)2(νC=O=1700cm-1,νO-H=3250-2500cm-1)如乙醇:CH3CH2OH(νO=H=3640cm-1)(CH3CH2OH)2(νO=H=3515cm-1)(CH3CH2OH)n(νO=H=3350cm-1)3)振动耦合(Coupling)当两个振动频率相同或相近的基团相邻并由同一原子相连时,两个振动相互作用(微扰)产生共振,谱带一分为二(高频和低频)。如羧酸酐分裂为νC=O(νas1820、νs1760cm-1)4)费米共振当一振动的倍频与另一振动的基频接近(2νA=νB)时,二者相互作用而产生强吸收峰或发生裂分的现象。COClνAr-C(δ)=880-860cm-1νC=O(as)=1774cm-11773cm-11736cm-15)空间效应由于空间阻隔,分子平面与双键不在同一平面,此时共轭效应下降,红外峰移向高波数。COOCCH3CH3νC=O=1663cm-1CH3νC=O=1686cm-1空间效应的另一种情况是张力效应:四元环>五元环>六元环。随环张力增加,红外峰向高波数移动。6)物质状态及制样方法通常,物质由固态向气态变化,其波数将增加。如丙酮在液态时,νC=O=1718cm-1;气态时νC=O=1742cm-1,因此在查阅标准红外图谱时,应注意试样状态和制样方法。7)溶剂效应极性基团的伸缩振动频率通常随溶剂极性增加而降低。如羧酸中的羰基C=O:气态时:νC=O=1780cm-1非极性溶剂:νC=O=1760cm-1乙醚溶剂:νC=O=1735cm-1乙醇溶剂:νC=O=1720cm-1因此红外光谱通常需在非极性溶剂中测量。3.3红外光谱仪目前有两类红外光谱仪:色散型和傅立叶变换型(FourierTransfer,FT)一、色散型:与双光束UV-Vis仪器类似,但部件材料和顺序不同。调节T%或称基线调平器置于吸收池之后可避免杂散光的干扰色散型红外光谱仪工作原理若单色光不被试样吸收,检测器中无交流讯号产生;若两束光的强度有差异——通过交流放大器放大,驱动光楔进行补偿;试样对某一波长的红外光吸收越多,光楔就越多地遮住参比光路以使两束光重新处于平衡;光楔部位的改变相当于试样的百分透光度。两束光经过单色器时,斩光器周期地切割两束光,使试样光束和参比光束交替地进入单色器中的色散棱镜或光栅,最后进入检测器。类型制作材料工作温度特点Nernst灯Zr,Th,Y氧化物o1700C-1高波数区(>1000cm)有更强的发射;稳定性好;硅碳棒SiCo1200-1500C低波数区光强较大;波数范围更广;坚固、发光面积大。1.光源常用的红外光源有Nernst灯和硅碳棒。机械强度差;但价格较高。材料透光范围/m注意事项NaCl0.2-25易潮解、湿度低于40%KBr0.25-40易潮解、湿度低于35%CaF20.13-12不溶于水,用于水溶液CsBr0.2-55易潮解TlBr+TlI0.55-40微溶于水(有毒)2.吸收池红外吸收池使用可透过红外的材料制成窗片;不同的样品状态(固、液、气态)使用不同的样品池,固态样品可与晶体混合压片制成。3.单色器由色散元件、准直镜和狭缝构成。其中可用几个光栅来增加波数范围,狭缝宽度应可调。狭缝越窄,分辨率越高,但光源到达检测器的能量输出减少,这在红外光谱分析中尤为突出。为减少长波部分能量损失,改善检测器响应,通常采取程序增减狭缝宽度的办法,即随辐射能量降低,狭缝宽度自动增加,保持到达检测器的辐射能量的恒定。4.检测器及记录仪红外光能量低,因此常用热电偶、测热辐射计、热释电检测器和碲镉汞检测器等。以光栅为分光元件的红外光谱仪不足之处:1)需采用狭缝,光能量受到限制;2)扫描速度慢,不适于动态分析及和其它仪器联用;3)不适于过强或过弱的吸收信号的分析。光源发出的红外辐射,经干涉仪转变成干涉图,通过试样后得到含试样信息的干涉图,由计算机采集,并经过快速傅立叶逆变换,得到吸收强度或透光度随频率或波数变化的红外光谱图。干涉仪作用:将各种频率的光信号经干涉作用调制为干涉图函数,再由计算机通过傅立叶逆变换计算出原来的光谱特点:(1)扫描速度极快(1s);适合仪器联用;(2)不需要分光,信号强,灵敏度很高;(3)仪器小巧。二、傅立叶红外光谱仪它是利用光的相干性原理而设计的干涉型红外分光光度仪。仪器组成为:光源、迈克尔逊干涉仪、探测器和计算机红外光源摆动的凹面镜摆动的凹面镜迈克尔逊干扰仪检测器样品池参比池同步摆动干涉图谱计算机解析还原红外谱图M1IIIM2BSD傅里叶变换红外光谱仪工作原理图迈克尔逊干涉仪工作原理图单色光单色光二色光多色光单、双及多色光的干涉示意图多色干涉光经样品吸收后的干涉图(a)及其Fourier变换后的红外光谱图(b)内部结构3.4试样制备一、对试样的要求1)试样应为“纯物质”(>98%),通常在分析前,样品需要纯化;对于GC-FTIR则无此要求。2)试样不含有水(水可产生红外吸收且可侵蚀盐窗);3)试样浓度或厚度应适当,以使T在合适范围。二、制样方法液体或溶液试样1)沸点低易挥发的样品:液体池法。2)高沸点的样品:液膜法(夹于两盐片之间)。3)固体样品可溶于CS2或CCl4等无强吸收的溶液中。固体试样1)压片法:1~2mg样+200mgKBr——干燥处理——研细:粒度小于2µm(散射小)——混合压成透明薄片——直接测定;2)石蜡糊法:试样——磨细——与液体石蜡混合——夹于盐片间;(石蜡为高碳数饱和烷烃,因此该法不适于研究饱和烷烃)。3)薄膜法:高分子试样——加热熔融——涂制或压制成膜;高分子试样——溶于低沸点溶剂——涂渍于盐片——挥发除溶剂样品量少时,采用光束聚光器并配微量池。一、定性分析1.已知物的签定将试样谱图与标准谱图对照或与相关文献上的谱图对照。2.未知物结构分析如果化合物不是新物质,可将其红外谱图与标准谱图对照(查对)如果化合物为新物质,则须进行光谱解析,其步骤为:1)该化合物的信息收集:试样来源、熔点、沸点、折光率、旋光率等;2)不饱和度的计算:通过元素分析得到该化合物的分子式,并求出其不饱和度过Ω.n3−n12Ω=1+n4+3.5应用简介Ω=0时,分子是饱和的,分子为链状烷烃或其不含双键的衍生物;Ω=1时,分子可能有一个双键或脂环;Ω=3时,分子可能有两个双键或脂环;Ω=4时,分子可能有一个苯环。一些杂原子如S、O不参加计算。3)查找基团频率,推测分子可能的基团;4)查找红外指纹区,进一步验证基团的相关峰;5)通过其它定性方法进一步确证:UV-Vis、MS、NMR、Raman等。定性分析-不饱和度分子的不饱和度定义:不饱和度是指分子结构中达到饱和所缺一价元素的“对”数。如:乙烯变成饱和烷烃需要两个氢原子,不饱和度为1。计算:若分子中仅含一,二,三,四价元素(H,O,N,C),则可按下式进行不饱和度的计算:Ω=(2+2n4+n3–n1)/2n4,n3,n1分别为分子中四价,三价,一价元素数目。定性分析作用:由分子的不饱和度可以推断分子中含有双键,三键,环,芳环的数目,验证谱图解析的正确性。Ω=1双键or饱和环Ω=2Ω=4叁键苯(一个环加三个双键)GBT23801-2009中间馏分油中脂肪酸甲酯含量的测定红外光谱法.pdfNYT1841-2010苹果中可溶性固形物、可滴定酸无损伤快速测定近红外光谱法.pdfNYT2659-2014牛乳脂肪、蛋白质、乳糖、总固体的快速测定红外光谱法.pdfSNT2326-2009食品及油脂中反式脂肪酸含量的检测傅立叶变换红外光谱法.pdf3.6红外光谱在食品检验中的应用
提供色散型红外光谱仪工作原理,色散型红外光谱仪的工作原理会员下载,编号:1701026975,格式为 xlsx,文件大小为49页,请使用软件:wps,office Excel 进行编辑,PPT模板中文字,图片,动画效果均可修改,PPT模板下载后图片无水印,更多精品PPT素材下载尽在某某PPT网。所有作品均是用户自行上传分享并拥有版权或使用权,仅供网友学习交流,未经上传用户书面授权,请勿作他用。若您的权利被侵害,请联系963098962@qq.com进行删除处理。

 下载
下载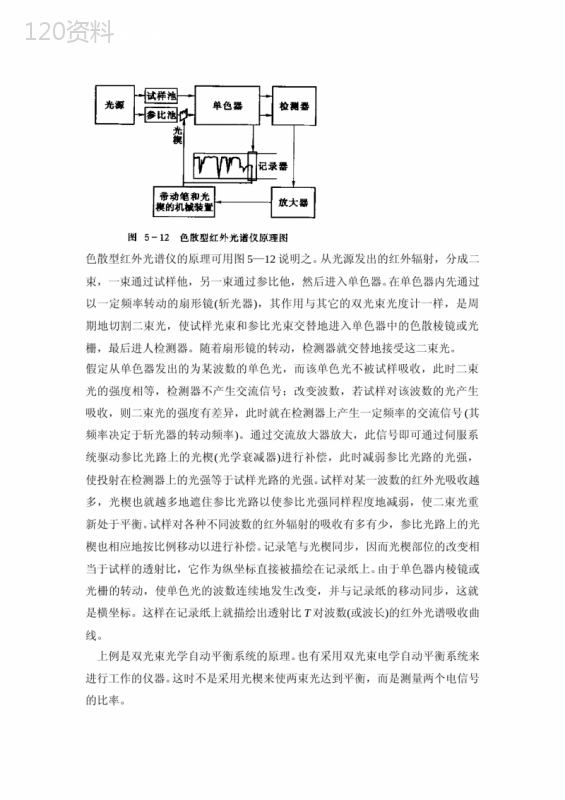 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载